納米二次離子質譜技術(NanoSIMS)在 微生物生態學研究中的應用
氮(N)、碳(C)、硫(S)等生命元素的生物地球化學循環過程主要由微生物所驅動。 耦合分析自然環境中 微生物遺傳多樣性與其代謝多樣性是當今微生物生態學研究的難點和熱點。 自然環境中的微生物多樣性極 為豐富,每噸土壤中的微生物類群可高達 400 萬種,海洋中的微生物類群也超過 200 萬種 。 實驗室富集分 離的傳統純培養方法對微生物生理生態功能的認識做出了巨大貢獻,但截止到 2003 年 7 月,全球范圍內僅分 離培養出 4800 種細菌 ,這極大地限制了人們對微生物功能多樣性的認識。 過去幾十年里,人們通過從環境 樣品中提取微生物 DNA 直接進行聚合酶鏈式反應(PCR),并利用 PCR 產物構建克隆文庫并進行測序分析, 發現了大量的未知序列。 通過將這些未知序列與已知的分離培養微生物序列進行比對,從而推測這些未培養 微生物的可能代謝類型,成為人們認識微生物多樣性和功能的重要手段。 但是,具有相似16S rRNA 基因組成 的類群不一定具有相同的代謝功能,豐度較高的微生物并不一定發揮更重要的生態功能,而且 PCR 反 應可能帶來一定的偏差,這成為基于 PCR 的分子生物學研究手段的主要缺陷。 考慮到微生物的廣泛分布及 其在元素地球化學循環中的重要作用,需要更先進的技術對自然環境樣品中的微生物群落和功能進行探測。
近年逐步興起的納米二次離子質譜技術(NanoSIMS)在國際上已被廣泛應用于地球科學、材料科學、比較 行星學、生物醫學和礦物學等領域,并在微生物生態學研究中顯示出巨大的潛力,是當前最為先進的表面和界 面分析技術,具有廣闊的應用前景。 通過利用穩定性或放射性同位素在原位或者微宇宙條件下標記目標微生 物,并與特異性的熒光原位雜交技術(FISH)、催化報告沉積熒光原位雜交技術(CARD-FISH)、鹵素原位雜交技術(HISH)等聯合應用,NanoSIMS 為從單細胞成像水平上研究復雜環境樣品中微生物群落的組成和代謝特 征提供了前所未有的可能性,其極高的靈敏度和準確性比其它的單細胞研究手段更具優勢。 本文將對納米二 次離子質譜的工作原理及其在微生物生態學研究領域的相關應用、存在的問題和發展趨勢等進行簡要介紹。
1 納米二次離子質譜技術(NanoSIMS)的原理
二次離子質譜技術(SIMS)是 20 世紀 70 年代發展起來的一種表面分析技術,它以一種離子(如 Cs +或 O - 初級離子束)轟擊固體表面,再將從表面濺射出來的次級離子引入磁場質量分析器, 不同離子根據質荷比不 同在靜電場區被分離開,經質譜檢測器檢測記錄并成像,得出被分析樣品表面的元素或化合物的組分。 SIMS 可以檢測從氫到鈾的所有元素、同位素和化合物,并以檢測原離子轟擊樣品表面產生的特征(“指紋冶)次級離 子譜為基礎的,因此既可提供樣品表面元素的信息,也可提供化學組分的信息,具有較高的空間分辨率和質量 分辨率。 SIMS 技術經歷了幾次更新,被廣泛應用于材料學、生物醫學、地質學和土壤學等領域。 SIMS 一般分 為靜態 SIMS 和動態 SIMS 兩種。 靜態 SIMS,例如飛行時間二次離子質譜(ToF-SIMS),根據測定激發的二 次離子飛行到接收器所用的時間來判斷離子種類,一般對樣品表面的一個到兩個原子層( < 1 nm)進行分析, 只能提供關于樣品淺層表面的信息,在應用于生態學研究時很難找到合適的條件同時滿足較高質量分辨率和 空間分辨率(一般只能達到微米級)的要求[7] ;而動態 SIMS 如 CAMECA IMS 1270-180 型、CAMECA IMS-3f-7f 型、及最先進的 CAMECA NanoSIMS 50L 型,主要根據二次離子在磁場中的偏轉半徑不同來確定離子種類,可 以獲得樣品表面幾微米內元素同位素分布和組成的信息(空間分辨率達到亞微米級或者納米級),成像水 平比靜態 SIMS 明顯提高,在微生物生態學中的應用也日漸成熟。
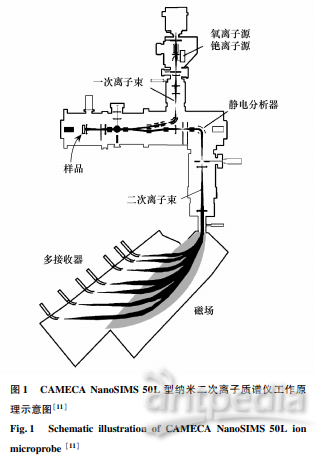
法國 CAMECA 公司生產的 NanoSIMS 50L 型是當前最為先進的動態二次離子質譜,相比于傳統的離子 探針具有極高的靈敏度和空間分辨率,其中銫(Cs + )離子源的分辨率達到 50 nm,氧(O - )離子源的分辨率達 到 150 nm,并且具有極高的質量分辨率,如能夠有效區分13C -與12C 1H - 、 12C 15N -與13C 14N -之間的細微質量差 異,并且能夠同時對 7 種離子進行成像分析和精確定 量。 CAMECA NanoSIMS 50L 與傳統的二次離子質 譜儀的工作原理非常相似,都是通過用一次離子束轟擊 的方式激發樣品表面產生二次離子,進而分析樣品表面 元素同位素組成和豐度。 具體工作流程為:首先將 離子源(Cs +或者 O - )產生的一次離子在真空加速器中 加速形成具有幾千電子伏特(KeV)的離子束,當這些高 能量的離子束聚焦并轟擊固體薄片樣品表面(微生物 細胞)時,濺射出樣品中的二次離子,這些具有不同荷 質比的二次離子由于在磁場中偏轉半徑不同而到達多 接收器的不同位置,然后通過接收器上的法拉第環或者 電子倍增器測量不同離子的強度,進而成像并通過圖像 定量分析軟件計算出樣品表面的元素同位素的豐度和 組成 信 息 ( 圖 1 )。 測 定 的 同 位 素 比 值 信 息 ( 例 如13C - / 12C - )不僅可以用于計算單細胞的元素吸收速 率,還可以表征元素的代謝途徑。 選擇合適的離子 源對于正確分析樣品信息極為關鍵,銫(Cs + )離子源激 發的負二次離子可以用來分析 C、CN、P、S、O、H 和鹵族 元素等,一般在微生物生態學研究中被廣泛采用,而氧 (O - )離子源激發的正二次離子適合于進行金屬的表面 分析。
2 納米二次離子質譜技術(NanoSIMS)應用于微生物生態學研究的技術路線
二次離子質譜技術(SIMS)在微生物生態學中的應用始于 2001 年。 Orphan 等首次利用 FISH 與 SIMS 結 合的方法證實了海洋沉積物中存在厭氧甲烷氧化古菌,能夠代謝13C—CH4。 但當時對同位素組成分析和 FISH 顯影分析需在不同的儀器上完成,而且 SIMS 的橫向分辨率較低,不能有效地對微生物的細胞進行辨 識,最新的 CAMECA NanoSIMS 50L 型二次離子質譜儀有效克服了這一難題。 應用 NanoSIMS 進行單細 胞成像分析的主要步驟為:在實驗室微宇宙培養或原位條件下,將采集的環境樣品或可培養的微生物暴露在 富含穩定性同位素( 15N 或13C 等)或者放射性同位素基質的環境中,經過短期的同位素標記過程之后,將樣品 進行固定、脫水,形狀不規則樣品需要用環氧樹脂包埋,絕緣的樣品(絕大多數微生物生態學研究樣品)需要 進行導電鍍膜( Au, Pt,Au / Pd 或者 C) 處理 ,制備成表面平整、符合儀器真空條件的薄片樣品進行 NanoSIMS 分析。 為了鑒別環境樣品中的目標微生物,NanoSIMS 需要與透射電子顯微鏡(TEM)、掃描電子顯 微鏡(SEM)、熒光原位雜交(FISH)、催化報告沉積熒光原位雜交(CARD-FISH)、鹵素原位雜交(HISH)、X 射 線能譜儀(EDS X-ray)等聯合使用來識別微生物的種類和功能(圖 2)。

3 納米二次離子質譜技術(NanoSIMS)的應用實例
3. 1 氮循環微生物
氮的生物地球化學循環主要由一系列微生物所驅動,識別并確定參與不同氮轉化途徑(包括固氮作用、 硝化作用、反硝化作用和氨化作用)的功能微生物是當前氮循環機制研究的核心問題之一。 NanoSIMS 技術在氮循環過程方面的應用首先在固氮微生物的研究上取得進展(表 1)。 2006 年,Lechene 等首次利用 NanoSIMS 從單細胞水平上研究并確定了實驗室純培養的固氮菌株 Teredinibacter turnerae 的固氮特性。 2007 年,Lechene 等又對與一種名為 Lyrodus pedicellatus 的船蛆(Shipworm)體內共生的固氮細菌進行了定量研 究。 由于船蛆本身的食物鏈中不包含氮元素,所以必須依靠與其共生的微生物提供氮源。 Lechene 等在實 驗室培養條件下向含有船蛆 Lyrodus pedicellatus 的海水中注入穩定性同位素底物15N2 ,然后經過 8d 的暴露培 養之后,先對樣品進行透射電子顯微鏡( TEM) 掃描確定待研究的船蛆組織中共生固氮細菌的位置,通過 NanoSIMS 分析后發現固氮細菌及周圍組織均被15N 所標記上,這直觀有力地提供了船蛆依賴固氮微生物獲取 氮源的證據。 這些早期利用 NanoSIMS 技術研究固氮微生物細胞功能的例子顯示出單細胞成像技術的巨 大應用潛力。
固氮微生物中另一類被廣泛研究的是絲狀藍藻,它們能夠同時固定 N2 和 CO2 ,其較大的細胞個體與獨特 的形態特征為 NanoSIMS 的應用提供了便利。 絲狀藍藻包括營養細胞和異型胞,但是過去由于研究手段的 限制,對氮元素和碳元素在這些細胞內及細胞之間的轉運和流動并不清楚。 Popa 等通過結合高分辨率的 NanoSIMS 與穩定性同位素標記技術對絲狀固氮藍藻 A. oscillarioides 的研究發現,新固定的氮元素可以被異型胞快速轉運,并最終分配到營養細胞中去。 此外,NanoSIMS 還可以根據細胞組織不同的元素組成從亞細胞 水平上進一步觀察絲狀藍藻 A. oscillarioides 體內的元素分布狀況。 另一個類似的通過 NanoSIMS 和 TEM 對固氮藍藻菌株 Trichodesmium 的研究發現了更為細致的13C 和15N 吸收的時空分布特征,其中 CO2 的固定速 率在上午達到最高水平,而 N2 的固定速率則在下午達到最高水平,并且新固定的 C 和 N 主要貯存在藻青素 顆粒中。 這些研究說明,將同位素標記技術與 NanoSIMS 和 TEM 成像技術聯合使用,能夠在探究微生物細 胞的生理組成元素及其相關代謝和轉運過程方面發揮巨大作用。 在最近的研究中它們用于分析兩種不同的 絲狀藍藻 Nodularia spumigena 和 Aphanizomenon sp. 對于波羅的海(Baltic Sea)碳氮循環的重要性,同時結合微 傳感器技術測定了兩種不同藍藻類群單細胞水平的氮固定和碳固定速率,從而能夠更加準確地估測不同碳氮 微生物對全球碳氮循環的貢獻率。
除了對實驗室純培養的固氮藍藻進行分析之外,NanoSIMS 同樣也能夠用于分析環境樣品中的固氮微生 物。 最近,Foster 等利用15N2 同位素標記與 NanoSIMS 結合的方法首次對寡營養海水中的 3 種硅藻-藍藻共生 體的單細胞固氮速率進行了測定,解決了過去由于技術手段限制不能夠將硅藻-藍藻共生體與其它固氮菌分 離研究的難題。 Halm 等通過 FISH 與 NanoSIMS 聯合使用,識別出在湖水厭氧層中發揮固氮作用的微生物 主要是數量非常少的綠硫細菌 Chlorobium sp.。 在更為復雜的河流沉積物樣品中,Dekas 等運用這 2 項技 術對具有甲烷厭氧氧化功能的古菌 ANME-2 和細菌 DSS 類群的聚合體進行了研究,在經過6 個月的15N2 同位 素培養實驗之后,根據15N 的吸收分布情況,發現這種聚合體中的 ANME-2 古菌具有固定氮氣的功能,并且能 夠將固定的氮元素轉運給 DSS 細菌。
近年來,隨著第一株具有氨氧化功能的古菌在實驗室獲得純培養,氨氧化古菌(AOA)作為除細菌以外硝 化作用的主要參與者,成為當前微生物生態學研究的熱點之一。 奧地利維也納大學的 Tourna 等成功地從 土壤中富集到了氨氧化古菌 Nitrososphaera viennensis,該菌株只有在添加有低濃度丙酮酸的培養基中才能將 NH + 4 轉化成 NO - 2。 為了驗證該菌是否利用丙酮酸中的 C 元素來合成細胞組織,他們在含有 N. viennensis 的培養基中加入13C 標記的丙酮酸,在 37 °C 培養 10 d 后運用 NanoSIMS 對樣品進行分析,發現大約有 10% 的 C 元素來自于13C-丙酮酸,其余的主要來自于對碳酸氫鹽的固定,證明 N. viennensis 具有化能自養和混合營養 生長的潛能。 該項研究是首次將 NanoSIMS 技術用于氨氧化微生物,對于探索新發現的氨氧化古菌的生理 代謝機制提供了新的思路。
3. 2 碳循環微生物
近些年發展起來的鹵素原位雜交(HISH)與 NanoSIMS 聯用的技術能夠分析環境樣品中的微生物組成,并 同時定量測定單細胞的代謝功能。 Musat 等首先將這種聯用技術用于研究寡營養湖水中 3 種厭氧光合細 菌 Chromatium okenii,Lamprocystis purpurea 和 Chlorobium clathratiforme 對 H 13CO - 3 和15NH + 4 的吸收特征。 他 們通過實驗室短期的微宇宙培養發現,同種光合細菌的不同細胞表現出極大的代謝速率差異,不同類群光合 細胞之間的差異更大。 其中,僅占細胞總數 0. 03% 的 C. okenii 貢獻了光合細菌碳吸收總量的 70% 和氮吸收 總量的40% ,這表明湖水中厭氧光合細菌的碳氮吸收過程主要是由一部分數量非常稀少的類群所完成的。
NanoSIMS 技術在碳循環微生物方面的另一類應用主要是對于甲基營養菌(包括甲醇營養菌和甲烷營養 菌)的研究。 Li 等利用碘標記的寡核苷酸探針原位雜交與 NanoSIMS 結合的方法對生物反應器中甲醇營養菌 的組成和功能進行了分析。 為了研究生物反應器系統中微生物吸收甲醇的機理,他們采用13C-甲醇培養采 自生物反應器的樣品,厭氧培養 25 d 后,首先用以碘標記的針對細菌和古菌的特異性探針確定樣品里的微生 物類群,然后將樣品固定用于 NanoSIMS 分析,結果發現古菌是生物反應器中吸收甲醇的主要功能微生物。 此外,Behrens 等運用類似的方法發現了口腔生物膜上的 Cytophaga-Flavobacterium 類群吸收13C-氨基酸的 功能。
3. 3 硫循環微生物
對 SRB 的種群組成和豐度進行了深入研究,但尚不能在單細胞水平解析其生理代謝功能特征。 近期,美 國研究者 Fike 等利用最新的 NanoSIMS 50L 型二次離子質譜儀,并結合 CARD-FISH 技術,成功地為解決這一 問題提供了新的視角,識別出在高鹽環境下微生物墊中參與硫循環的主要微生物類群是 Desulfobacteraceae 科 的硫酸鹽還原菌。 他們首先用外層包裹有35 SO4 的銀箔與微生物墊中可溶性的硫化物反應,由于硫化物 與35 SO4 的氧化還原反應使硫化物中的34 S 固定在銀箔表面,然后通過 NanoSIMS 成像技術就能夠測定樣品中 啄 34 S 同位素的組成情況,從而計算出不同微生物墊深度上硫化物的濃度。 NanoSIMS 所生成的二維圖像表明, 微生物墊 中 硫 化 物 的 濃 度 隨 著 深 度 的 增 加 而 減 少, 這 種 變 化 趨 勢 與 利 用 CARD-FISH 所 測 定 的 Desulfobacteraceae 科的硫酸鹽還原菌豐度隨微生物墊深度的變化趨勢相吻合,說明 Desulfobacteraceae 科對微 生物墊中硫化物的空間分布具有決定作用。 以往對于硫酸鹽還原菌的研究多停留在對其總的豐度和結構 組成分布上,而通過使用 NanoSIMS 與 CARD-FISH 結合的方法能夠將微生物的空間分布與硫化物的空間分布 聯系在一起,更容易識別硫酸鹽還原過程中的關鍵活躍類群。硫酸鹽還原菌(SRB)是硫元素生物地球化學循環過程的關鍵功能類群,經典的分子生物學研究手段已經對 SRB 的種群組成和豐度進行了深入研究,但尚不能在單細胞水平解析其生理代謝功能特征。 近期,美 國研究者 Fike 等利用最新的 NanoSIMS 50L 型二次離子質譜儀,并結合 CARD-FISH 技術,成功地為解決這一 問題提供了新的視角,識別出在高鹽環境下微生物墊中參與硫循環的主要微生物類群是 Desulfobacteraceae 科 的硫酸鹽還原菌。 他們首先用外層包裹有35 SO4 的銀箔與微生物墊中可溶性的硫化物反應,由于硫化物 與35 SO4 的氧化還原反應使硫化物中的34 S 固定在銀箔表面,然后通過 NanoSIMS 成像技術就能夠測定樣品中 啄 34 S 同位素的組成情況,從而計算出不同微生物墊深度上硫化物的濃度。 NanoSIMS 所生成的二維圖像表明, 微生物墊 中 硫 化 物 的 濃 度 隨 著 深 度 的 增 加 而 減 少, 這 種 變 化 趨 勢 與 利 用 CARD-FISH 所 測 定 的 Desulfobacteraceae 科的硫酸鹽還原菌豐度隨微生物墊深度的變化趨勢相吻合,說明 Desulfobacteraceae 科對微 生物墊中硫化物的空間分布具有決定作用。 以往對于硫酸鹽還原菌的研究多停留在對其總的豐度和結構 組成分布上,而通過使用 NanoSIMS 與 CARD-FISH 結合的方法能夠將微生物的空間分布與硫化物的空間分布 聯系在一起,更容易識別硫酸鹽還原過程中的關鍵活躍類群。
3. 4 其它方面的應用 NanoSIMS 技術除了在氮、碳、硫等元素的生物地球 化學循環研究中得到廣泛應用外,研究者們也在不斷拓 展著 NanoSIMS 在微生物生態學方面的應用范圍。 微 生物的空間分布及其在土壤基質中的功能活性對于元 素地球化學循環具有極為重要的影響,而且土壤的高度 異質性為微生物提供了無數性質各異的微環境,將 土壤理化環境的異質性與其對生物過程的影響聯系起 來是當今土壤微生物生態學的研究前沿之一,然而 過去的技術手段對于分析微生物與土壤基質接觸的生 物物理界面無能為力。 2007 年,Herrmann 等創新地將 NanoSIMS 運用于土壤微生物的活性與空間分布的研 究,并同時觀察了土壤物理微環境對于微生物的影 響。 他們首先將土壤中廣泛分布的 Pseudomonas fluorescens 的純培養菌株(NCTC10038)在含有15NH + 4 的 培養基中進行標記 24 h 后,混入土壤樣品中,然后用環 氧樹脂固定并切片供 NanoSIMS 觀察。 其中, 28 Si -離子 成像圖用來表示土壤基質的組成, 12C -成像圖表示樹脂 的 組 成, 12C 14N - 成 像 圖 表 示 含 氮 有 機 質, 12C 15N - 與12C 14N -的比值(即15N/ 14N)可以表示15N-P. fluorescens 的分布(圖 3)。

從 NanoSIMS 成像圖中,可以清晰地 看到15N 標記的 P. fluorescens 主要分布在土壤粒子的邊緣部分。 該項研究顯示出 NanoSIMS 在分析微生物 在土壤中的微域分布及其與土壤基質相互作用方面的巨大可能性。 類似的研究方法已經開始用于對土壤微生物-植物相互作用的研究。 Clode 等利用 NanoSIMS 在原位狀態下研究了15N 元素在土壤根際圈的轉運情 況,并重點關注了植物細胞與根際微生物對 N 元素的相互競爭。 這種原位研究元素流動的高分辨率成像 方法顯示了 NanoSIMS 在分析復雜土壤環境中微生物過程的優越性,而以往的此類研究只能主要依靠簡單的 數學模型分析。 NanoSIMS 在微生物生態學方面的其它可能應用還包括:控制土壤礦物質表面磷肥固定的微 生物機理,促進有機質在土壤中穩定化過程的微生物類群,土壤基質中微生物與特定礦物質的相互作用,土壤 中目標微生物活躍類群的空間分布,影響微生物水平基因轉移的微觀尺度因素等。
4 使用 NanoSIMS 技術應注意的問題

4. 1 樣品制備 樣品制備是 NanoSIMS 分析中極為關鍵的環節,因為 NanoSIMS 一般在超高真空環境中進行操作,因此制備的環境樣品必須充分脫水并且能夠承受真空。 樣品脫水的方法一般包括化學固定液(如加入乙醇、甲醛或 戊二醛等)、低溫脫水、環氧樹脂包埋等。 不同的脫水方法適用于不同樣品的 NanoSIMS 分析,如果 在樣品制備的過程中待分析的元素有可能發生轉移和流動,最好使用低溫脫水方法來固定樣品的形態,例如 在研究固氮微生物的碳氮吸收途徑的時候 。 對于形狀不規則的樣品最好用樹脂進行包埋,然后切成薄 片狀以便進行 NanoSIMS 分析。 甲醛固定液對于微生物細胞的蛋白質、脂質和核酸有非常有效的固定和脫水 作用 ,但是在固定的過程中也有可能引入微生物細胞中的12C,從而使 NanoSIMS 的分析出現一定的偏差。 尤其是當 NanoSIMS 與熒光雜交技術如 FISH、CARD-FISH 和 HISH 聯用時,最好使用多聚甲醛對樣品進行脫 水處理 。 Peteranderl 和 Lechene 比較了低溫脫水與化學固定對樣品制備的不同影響,發現化學固定導致二 次離子12C -和12C 14N -的產率降低,并且化學固定液有可能洗脫低分子量的細胞組織。 而 Ploug 等對這 2 種脫水方法的研究表明,化學固定法并沒有顯著地影響待測樣品的元素組成。
4. 2 微生物的識別
在 NanoSIMS 分析中,不同的二次離子能夠表征樣品的不同組成,因此如何正確地將離子成像信息與微 生物類群聯系起來顯得非常關鍵。 例如在固氮硅藻-藍藻共生體的研究中就會遇到類似的難題,因為共生藍 藻細胞經常生長在硅藻的細胞壁與細胞膜之間,為有效區分這兩種不同微生物對 N 的吸收帶來較大困難,因 此在 NanoSIMS 分析之前必須首先破壞去除硅藻的細胞壁,然后再進行下一步分析。 識別復雜環境樣品中 的微生物類群也可以通過在 NanoSIMS 分析之前首先進行 FISH 或者 CARD-FISH 分析,以此確定微生物的組 成和種類,但是將熒光原位雜交的圖像與 NanoSIMS 分析的圖像正確地聯系在一起也是非常艱難的工作。 為 了有效地對微生物進行識別,在 NanoSIMS 分析之前也最好輔之以 TEM 或者 SEM 等電子顯微鏡技術對樣品 進行必要的基本特征分析,首先確定好適合 NanoSIMS 分析的感興趣區域,這樣可以節省大量的時間。 例如 在分析富含有機質的沉積物樣品中的微生物群落時,有機質濃度較高的區域往往也是微生物富集的區域,因 此首先用電子顯微鏡確定有機質的分布區域,可以更加快速地找到目標微生物。
5 總結和展望
以 NanoSIMS 為代表的單細胞分析技術的興起為研究微生物生態學提供了嶄新的機遇,并且已經在參與 氮、碳、硫等元素生物地球化學循環的微生物研究中顯示出前所未有的優勢和重要的應用前景。 NanoSIMS 不 僅能夠提供微生物的生理生態特征信息,而且能夠確定并識別復雜環境樣品中的代謝活躍的微生物細胞,并 將其類群信息與功能聯系起來,對于從微觀尺度上識別不同微生物群落在元素循環中的作用和在生態系統中 的功能具有重要意義。 然而,NanoSIMS 技術本身依舊存在很多問題:(1)在進行 NanoSIMS 分析時,如果選 擇反映同位素富集的感興趣區域不合適,可能會影響對微生物功能的正確分析;(2)在制備可供 NanoSIMS 分 析的樣品時,固定和脫水等過程可能會對微生物細胞的同位素組成造成一定的影響;(3)由于 NanoSIMS 一般 與同位素標記技術聯合使用,標記過程中微生物交叉取食和同位素被稀釋的風險同樣也會影響后續的 NanoSIMS 分析結果。 (4)由于 FISH 技術應用于復雜土壤樣品的難題,NanoSIMS 與 FISH 聯用仍然很難區分 不同類群土壤微生物的功能活性。 當前微生物生態學的研究技術多基于 PCR 擴增,對環境微生物的認識以 易于被 PCR 擴增出的優勢種群為主,對環境中豐度較低的稀有微生物種群認識嚴重不足,未來基于 NanoSIMS 的研究方法將有助于揭示自然環境豐度較低但發揮重要功能作用的微生物種群。 同時,隨著原位 雜交技術的進一步發展,結合不斷豐富的生物標志物,如脂類、DNA/ RNA、蛋白質等,NanoSIMS 將可能為研究 微生物的類群和功能提供更為完整的信息。